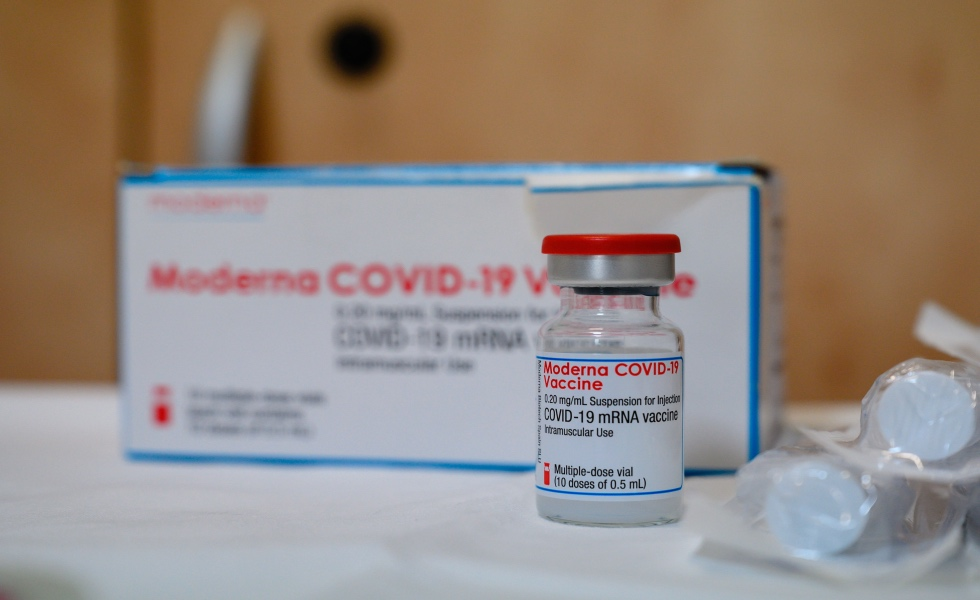
El Instituto Nacional de Vigilancia de Medicamentos y Alimentos, Invima, aprobó este lunes la solicitud de la modificación de uso de emergencia de la vacuna contra la Covid-19 elaborada por la farmacéutica Moderna.
El instituto expresó que esta decisión se soporta en los datos de seguridad recopilados en el estudio clínico realizado en Estados Unidos, el cuál contó con la participación de más de 3.000 pacientes de 12 a 17 años de edad.
“En ese sentido, la nueva indicación del biológico para la inmunización activa es para personas mayores de 12 años, en una serie de 2 dosis (0,5 ml cada una), administrada intramuscularmente. Cada dosis de la vacuna contiene 0.5 ml con 100 microgramos de ARN mensajero, que codifica proteína del virus SARS-CoV-2”, explicó Invima.
Des esta forma, Moderna se une a Pfizer en ser las únicas farmacéuticas aprobadas por el Instituto para la aplicación de sus biológicos en los jóvenes de edades entre los 12 y 17 años.